Einfach hineinzwängen: Unterschied zwischen den Versionen
K (Textersetzung - „<seo description="“ durch „{{#seo:|description=“) |
|||
| Zeile 35: | Zeile 35: | ||
| − | {{#seo:|description=Ionen, Naturgesetze Coulombwall Coulombsche Ordnung Nanotechnologie, Drexel University, Yury Gogotsi, Kohlenstoffnanomaterial Kohlenstoffnanoporen Ionische Flüssigkeit Elektrolyt Spiegelladung alternierende Ladungen | + | {{#seo:|description=Ionen, Naturgesetze Coulombwall Coulombsche Ordnung Nanotechnologie, Drexel University, Yury Gogotsi, Kohlenstoffnanomaterial Kohlenstoffnanoporen Ionische Flüssigkeit Elektrolyt Spiegelladung alternierende Ladungen}} |
{{SORTIERUNG:Einfach hineinzwängen}} | {{SORTIERUNG:Einfach hineinzwängen}} | ||
Version vom 1. Oktober 2022, 16:36 Uhr
Forscher von der Drexel University haben entdeckt, dass die Natur ihre Gesetze lockert, wenn die Räume eng werden
Es hat sich herausgestellt, dass Ionen, wenn sie es denn besonders eilig haben und der zur Verfügung stehende Raum begrenzt ist, ebenso wie Menschen einen Weg finden, sich hineinzuzwängen – selbst wenn dies erfordert, sich den Gesetzen der Natur zu widersetzen. Kürzlich veröffentlichte Forschungsergebnisse eines internationalen Wissenschaftlerteams, zu dem auch Yury Gogotsi, PhD, von der Drexel University gehört, haben gezeigt, dass geladene Teilchen tatsächlich auf ihr Verhalten nach dem Prinzip des „Gegensätze ziehen sich an“, der sogenannten Coulombschen Ordnung, verzichten, wenn sie in den winzigen Hohlräumen eines Nanomaterials eingeschlossen sind. Diese Entdeckung könnte eine entscheidende Weichenstellung für die Energiespeicherung, die Wasseraufbereitung sowie für alternative Technologien zur Energieerzeugung darstellen, bei denen Ionen in nanoporösen Materialien eingeschlossen sind.

In ihrer Arbeit, die kürzlich in der Zeitschrift Nature Materials veröffentlicht wurde, erklären die Forscher, wie die Coulombsche Ordnung in flüssigen Salzen zerfällt, wenn Ionen in kleinen Räumen eingeschlossen sind – insbesondere in Kohlenstoffporen von weniger als einem Nanometer Durchmesser. Und je enger die Poren sind, desto weniger halten sich die Ionen an die Coulombsche Ordnung.
„Es ist dies das erste Mal, dass es gelungen ist, die Aufhebung der Coulombschen Ordnung in Subnanometerporen überzeugend aufzuzeigen“, sagte Gogotsi, einer der Autoren der Studie, seines Zeichens Distinguished University sowie Charles T. and Ruth M. Bach Professor am Drexel College of Engineering. „Das Brechen von Symmetrieprinzipien, wie etwa die Coulombsche Ordnung, spielt in der Natur eine wesentliche Rolle. Aber viele dieser Prozesse laufen ab, ohne dass wir sie überhaupt verstehen und ihre Mechanismen kennen. Die Wissenschaft hat die Möglichkeit, diese verborgenen Prozesse aufzudecken. Und wenn wir sie dann verstehen, können wir letztendlich erfolgversprechendere Technologien entwickeln, indem wir auf denselben Skalen im Nanometer- und Subnanometerbereich arbeiten, so wie die Natur es tut“.
Um zu seiner Entdeckung zu gelangen, hatte das Team, zu dem auch Forscher der Shinshū-Universität in Japan, der Loughborough University im Vereinigten Königreich, der University of Adelaide in Australien sowie der Universität Sorbonne, des französischen Forschungsnetzwerkes für elektrochemische Energiespeicherung und der Universität Paul Sabatier in Frankreich gehören, zwei Sätze von Kohlenstoffnanomaterialien entwickelt. Einer von ihnen wies Poren mit einem Durchmesser von mindestens einem Nanometer auf, der andere Poren von unter einem Nanometer. Anschließend benutzten sie diese Materialien, um mit ihnen ionische Flüssigkeiten aufzusaugen, so als handele es sich um einen Schwamm, der Wasser aufsaugt.
Bei derartigen ionischen Flüssigkeiten, bei denen es sich um Salze handelt, die bei Raumtemperatur in flüssigem Zustand vorliegen und die in der chemischen Industrie häufig als Lösungsmittel verwendet werden, befinden sich die Ionen in Schichten, die dem alternierenden Positiv-Negativ-Muster der Coulombschen Ordnung entsprechen. Sobald die ionische Flüssigkeit jedoch in die Kohlenstoffnanoporen eingedrungen war, waren die Ionen gezwungen, sich in ein- und zweireihigen Gruppen anzuordnen. Gleich einer Horde von Grundschülern, die auf den Bus zu rennen, standen sie dann in der Schlange jedoch nicht mehr zwangsläufig neben ihren gewohnten Mitschülern.
„In diesem Zustand ist die Coulombsche Ordnung der Flüssigkeit aufgehoben“, schreiben die Autoren. „Ionen mit gleicher Ladung grenzen sich infolge einer Abschirmung ihrer elektrostatischen Wechselwirkungen, welche durch die in den Porenwänden induzierten Spiegelladungen hervorgerufen wird, gegenseitig voneinander ab.“
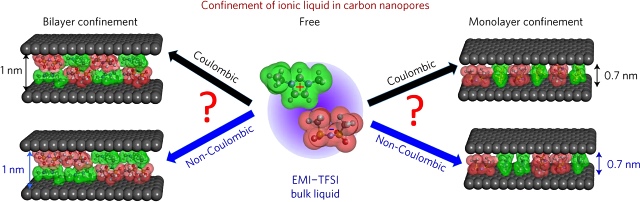
Beobachtet hat das Team diese Störung der natürlichen Ordnung der Ionen mit Hilfe der Röntgenstreuung. Um diese experimentellen Beobachtungen zu verdeutlichen, haben sie den Prozess in einem Modell nachgebildet. Außerdem berichteten sie, dass die nichtcoulombsche Ordnung noch wesentlich ausgeprägtere Formen angenommen hat, wenn das Kohlenstoffmaterial mit einer elektrischen Ladung beaufschlagt wurde.
„Unsere Ergebnisse deuten auf die Existenz eines Mechanismus auf molekularer Ebene hin, der die Coulombsche Abstoßungsenergie zwischen Co-Ionen, die sich einander annähern, verringert“, schreiben sie. Dieser Mechanismus, so die Theorie, hängt mit jener Ladung zusammen, mit der die Wände der Kohlenstoffporen vorübergehend aufgeladen werden. Diese „Spiegelladung“, so schreiben sie, hebe die natürliche elektrostatische Abstoßung zwischen Ionen gleicher Ladung auf, so dass sich die Kanäle mit Ionen gleicher Ladung füllen können und diese dann direkt nebeneinander angeordnet sind.
Gogotsi weist darauf hin, dass diese Entdeckung die Verwendung von ionischen Flüssigkeiten in Batterien und anderen Energiespeichern erleichtern könnte. So wurde diese Methode bereits dahingehend untersucht, Batterien mit ihrer Hilfe sicherer zu machen. Dies hat sich jedoch noch nicht durchsetzen können, weil hierdurch die Leistungsfähigkeit der Batterien eingeschränkt wird.
„Wir können sicherere Batterien und Superkondensatoren dadurch erzielen, dass wir ionische Flüssigelektrolyte verwenden, denn diese sind nicht entflammbar – ganz im Gegensatz zu jenen Elektrolytlösungen, die derzeit noch in diesen Geräten zum Einsatz kommen“, so Gogotsi. „Da hier keine Lösungsmittel enthalten sind, nehmen die Ionen das gesamte Volumen ein, wodurch sich möglicherweise eine größere Menge an Energie speichern lässt als in herkömmlichen Elektrolyten, in denen organische Lösungsmittel enthalten sind.“
Er geht davon aus, dass diese Entdeckung auch einen bedeutenden Einfluss auf die Technologie zur Wasserentsalzung haben könnte. Mit diesem Wissen über das Verhalten von Ionen in Subnanometerporen könnten die Membranen, die derzeit entwickelt werden, um Salzwasser in Trinkwasser zu verwandeln, weiter verbessert werden.
„Diese Arbeit trägt zu einem grundlegenden Verständnis darüber bei, wie sich verschiedene Dinge im Größenbereich unterhalb eines Nanometers verhalten können“, so Gogotsi. „Damit gehen wir über die Nanotechnologie hinaus und stoßen in den Bereich subnanoskaliger Prozesse vor – dieser bildet für uns nun die nächste Grenze.“
